
Si pudieses acercarte y mirar tu ADN, ¿qué crees que verías? Seguramente te imaginas cientos de genes, o quizá se te viene a la mente alguna de las secuencias de ADN que nos suelen enseñar gráficamente cuando buscamos esta palabra en internet.
Lo cierto es que lo que realmente te encontrarías es una sola secuencia, la TTAGGG, repetida una y otra y otra vez, cientos e incluso miles de veces. El ADN está formado por desoxirribonucléotidos, cadenas de nuclóetidos, donde cada unidad está constituida por tres partes: una molécula de azúcar de 5 carbonos, un grupo de fosfato y 4 bases nitrogenadas.
Otra de las partes más importantes del ADN y de los cromosomas son los telómeros y la telomerasa, que, además, tienen un papel esencial en el envejecimiento. ¿Quieres saber más sobre estas estructuras? ¡Te lo contamos en este artículo!
¿Qué es un telómero y cuáles son sus funciones?
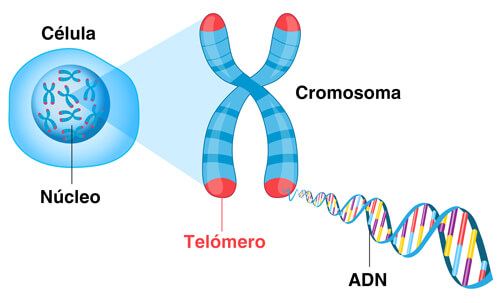
Los telómeros son estructuras distintivas que se encuentran en los extremos de los cromosomas, es decir, la “punta del cromosoma” y consiste en la misma secuencia corta de ADN que repite una y otra vez. En los seres humanos, la secuencia de los telómeros es TTAGGG y suele repetirse unas 3.000 veces, llegando alcanzar hasta 15.000 pares de bases en longitud.
 Básicamente, los telómeros tienen tres propósitos principales:
Básicamente, los telómeros tienen tres propósitos principales:
- Ayudar a organizar cada uno de los 46 cromosomas en el núcleo de las células.
- Proteger los extremos de los cromosomas formando una tapa, muy parecida a la punta de plástico de los cordones de zapatos.
- Permitir que el cromosoma se replique correctamente durante la división celular.
Como acabamos de mencionar, para evitar la pérdida de genes a medida que se desgastan los extremos de los cromosomas, las puntas de los cromosomas eucariotas tienen “tapas” de ADN especializadas, que son los telómeros.
Cada vez que una célula se divide, es necesario duplicar cada cromosoma para proporcionar una copia de la información genética de la nueva célula. No obstante, el final del cromosoma no se puede copiar, por lo que, cada vez que se duplica, los telómeros se acortan. Este acortamiento también se ha relacionado con el envejecimiento de las células y podrían explicar por qué las células solo pueden dividirse un cierto número de veces.
De esta forma, los telómeros actúan como un amortiguador para garantizar que la información genética importante codificada en el cromosoma esté protegida y no se pierda durante la replicación. De hecho, para proteger esta información, los telómeros críticamente cortos actúan como una señal para que la célula deje de dividirse.
Cuando los telómeros se quedan tan pequeños que ya no pueden proteger el ADN, las células dejan de reproducirse y alcanzan un estado de vejez. Por eso, la longitud de los telómeros se considera un “biomarcador de envejecimiento” clave a nivel molecular.
Entonces, ¿qué es la telomerasa?
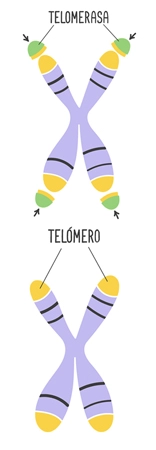
Ahora que ya sabemos qué son los telómeros y cuáles son sus funciones, toca hablar de la telomerasa. Se trata de la enzima responsable del mantenimiento de la longitud de los telómeros mediante la adición de secuencias repetitivas ricas en guanina, es decir, agrega la secuencia de telómeros TTAGGG a los extremos de los cromosomas.
 Además del alargamiento catalítico de los telómeros, las funciones independientes de la telomerasa también pueden participar en la regulación del ciclo celular. Por otro lado, la formación de enzima temporalmente activa, a través de su activación intracelular o debido a la estimulación de la expresión de los componentes de la telomerasa, da como resultado la activación de esta enzima y el alargamiento de los telómeros que pueden usarse para corregir cambios degenerativos.
Además del alargamiento catalítico de los telómeros, las funciones independientes de la telomerasa también pueden participar en la regulación del ciclo celular. Por otro lado, la formación de enzima temporalmente activa, a través de su activación intracelular o debido a la estimulación de la expresión de los componentes de la telomerasa, da como resultado la activación de esta enzima y el alargamiento de los telómeros que pueden usarse para corregir cambios degenerativos.
La telomerasa solo se encuentra en concentraciones muy bajas en las células somáticas (células del cuerpo) y, debido a que estas células no usan telomerasa con regularidad, envejecen, lo que lleva a una reducción de la función normal. Precisamente, el resultado de este envejecimiento es que el propio cuerpo humano también envejece.
Por el contrario, la telomerasa se encuentra en niveles altos en la línea germinal (las células que producen los óvulos y el esperma) y células madre. Estos son tipos de células que necesitan sufrir muchas divisiones o, en el caso de las células germinales, dar lugar a un nuevo organismo. Así pues, la longitud de los telómeros se mantiene después de la replicación del ADN y las células no muestran signos de envejecimiento.
Además, curiosamente, muchas células cancerosas tienen telómeros acortados y la telomerasa está activa en estas células, lo que permite que este tipo de células sean inmortales y continúen replicándose. Si la telomerasa pudiese ser inhibida por fármacos como parte de la terapia contra el cáncer, los telómeros se acortarían hasta alcanzar una “longitud crítica”, lo que evitaría esa división excesiva (y, por tanto, el crecimiento del tumor canceroso).
¿Qué ocurre cuando el proceso no funciona bien?
En algunas personas, este proceso de los telómeros no funciona bien, quizá porque estos son intrínsecamente más cortos o porque se acelera el proceso de acortamiento. De hecho, podría ser incluso una combinación de ambos.
También puede ser que sea la enzima telomerasa la que no funcione correctamente y no mantenga una longitud del telómero saludable o la estructura protectora es defectuosa.
 En los trastornos de la biología de los telómeros, la extensión, replicación o mantenimiento de la longitud o estructura se ven afectados. La gama de síntomas es variada, ya que las células con telómeros cortos pueden afectar a cualquiera de los órganos del cuerpo. Por ejemplo, en el caso de la fibrosis pulmonar, los principales afectados son los pulmones. En personas con disqueratosis congénita, la insuficiencia de la médula ósea es uno de los más comunes.
En los trastornos de la biología de los telómeros, la extensión, replicación o mantenimiento de la longitud o estructura se ven afectados. La gama de síntomas es variada, ya que las células con telómeros cortos pueden afectar a cualquiera de los órganos del cuerpo. Por ejemplo, en el caso de la fibrosis pulmonar, los principales afectados son los pulmones. En personas con disqueratosis congénita, la insuficiencia de la médula ósea es uno de los más comunes.
Lo cierto es que hay un número creciente de mutaciones genéticas conocidas que dan resultados telómeros cortos y trastornos de la biología de los telómeros, pero en un número significativo de casos todavía no se conoce la causa.
En estos casos, las pruebas de longitud de los telómeros pueden desempeñar un papel vital en el diagnóstico y la gestión del tratamiento. Una de estas pruebas es la técnica de hibridación in situ cuantificada (Q-FISH), que mide la longitud en núcleos en interfase de células sanguíneas mediante el marcaje con una sonda telómerica fluorescente.
Cada sonda reconoce un número fijo de repeticiones teloméricas, por lo que la intensidad de la fluorescencia que emite es directamente proporcional a la longitud del mismo.
¿Cuál es la importancia de los telómeros en la medicina?
Hasta el momento, no son muchas las investigaciones que se han realizado sobre la telomerasa y los telómeros, pero lo que sí se sabe es que su investigación y el papel de esta enzima podrían revelar información muy valiosa para combatir el envejecimiento y el cáncer.
Los resultados de varios estudios sugieren que el acortamiento de los telómeros constituye un mecanismo importante que limita la vida útil de las células. Este es uno de los mecanismos desencadenantes del envejecimiento celular mejor caracterizados, que se acelera considerablemente por el estrés oxidativo.
 No obstante, la relevancia médica de los telómeros es incierta, ya que se ha observado que las células humanas en el laboratorio dejan de dividirse cuando se inactiva la telomerasa, porque la longitud de los telómeros no se mantiene después de la división celular.
No obstante, la relevancia médica de los telómeros es incierta, ya que se ha observado que las células humanas en el laboratorio dejan de dividirse cuando se inactiva la telomerasa, porque la longitud de los telómeros no se mantiene después de la división celular.
Posteriormente, las células entran en un estado de inactividad, llamado senescencia y, una vez se reactiva la telomerasa, estas células pueden continuar dividiéndose.
Si la telomerasa puede usarse para ayudar a las células humanas a vivir para siempre, también puede ser posible producir células en masa para trasplantes, que podrían ayudar a prevenir una variedad de afecciones, desde quemaduras hasta diabetes.
Además, los mecanismos de senescencia celular ayudan a entender el envejecimiento de los tejidos y el proceso hacia la muerte, pero el verdadero reto, a día de hoy, es salvar todas aquellas vidas que penden de un hilo por un grupo de células rebeldes, y, como hemos dicho anteriormente, la telomerasa tienen un papel importante en las células cancerosas.
 Llámanos
Llámanos
